Андрей Папиш
|37
Американские химики в ходе экспериментов с пептидами обнаружили новое объяснение гомохиральности молекул, из которых строится жизнь. Оно основано на дисбалансе односторонних молекул в исходном составе.
Биологические молекулы в большинстве своем хиральны — то есть у них есть зеркальная копия, как у левой ладони есть копия в виде правой. Такие пары существуют в виде энантиомеров, то есть стереоизомеров, устроенных одинаково, но не совмещающихся в пространстве. Однако у молекул, из которых строится жизнь, по неизвестной причине нет хиральных дубликатов. Эту характерную черту называют гомохиральностью или хиральной чистотой. Если в обычных химических реакциях две смеси с лево- или правосторонними молекулами (рацемические смеси) в целом идентичны, то в биологических — наоборот. Смесь из молекул с измененной конфигурацией будет инертна или вовсе токсична, то есть останется «неживой».
Ученые давно пытаются понять, почему молекулы жизни — аминокислоты, углеводы, пептиды — почти всегда встречаются только в односторонней форме. Структуры ДНК и РНК, а также белки построены из молекул, у которых нет пары стереоизомеров: только левовращательные L-аминокислоты и правовращательные D-нуклеотиды. Сами ДНК закручены только в левую сторону. Предполагали, что гомохиральность зависит от разницы физических свойств молекул. Также высказывалась версия, что все дело в случайном нарушении синтеза исходных для молекул веществ.
Новое исследование, опубликованное в журнале Nature, предлагает другое объяснение этой загадки. Химики из американского исследовательского центра The Scripps Research Institute синтезировали наборы пептидов и рассмотрели механизмы хирального усиления в гомохиральном и гетерохиральном реагентах.
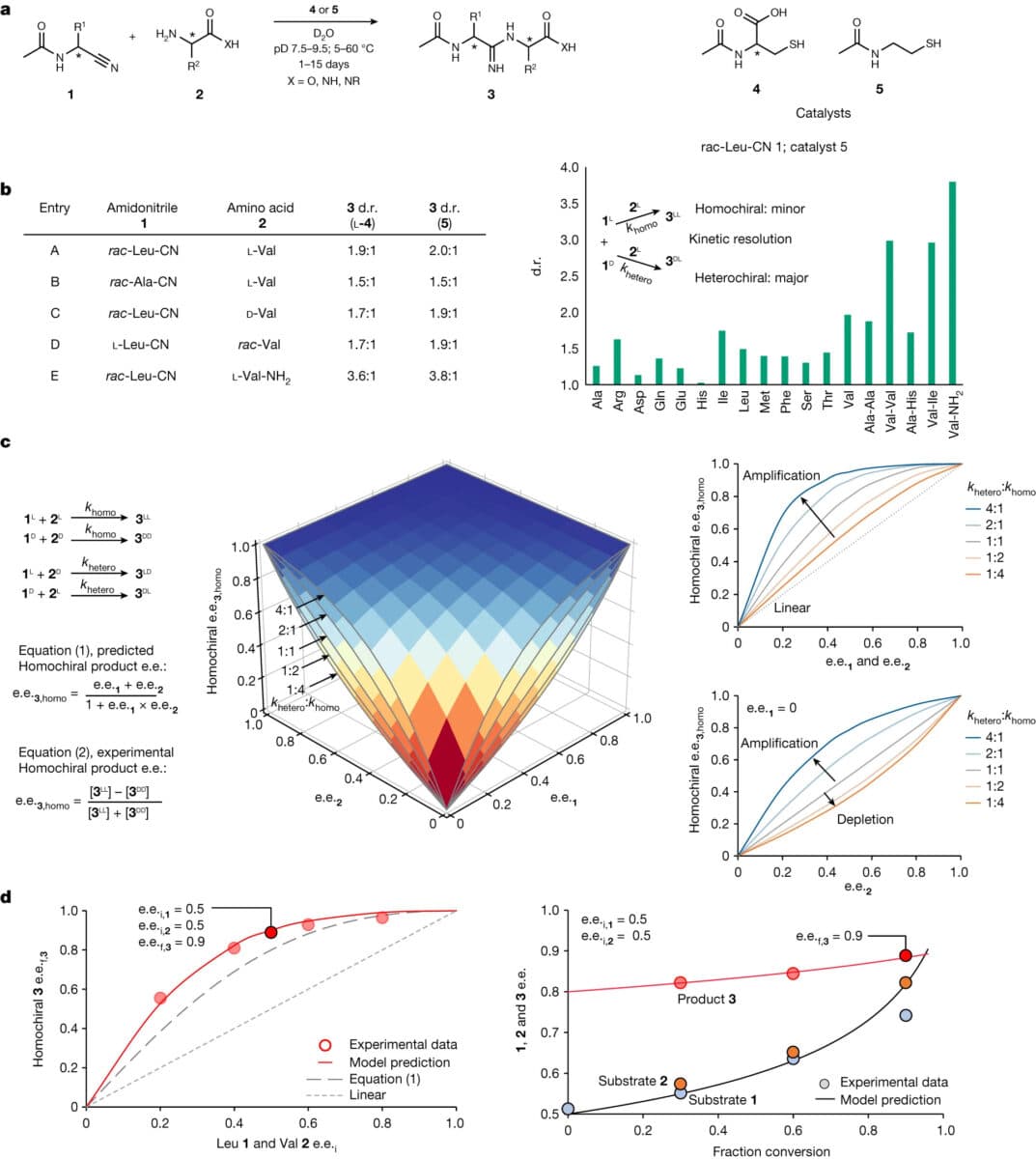
Сначала исследователи создали дипептидный продукт, то есть соединили две разные аминокислоты при помощи добавления в раствор тиола (по-другому реакция называется лигированием). Авторы не изобрели эту реакцию, но впервые рассмотрели ее с точки зрения возникновения гомохиральности.
В ходе эксперимента выяснилось, что если в процессе образования дипептида в смеси наблюдался дисбаланс энантиомеров в левую сторону, то симметрия нарушалась и молекулы, количество молекул, закрученных налево, доминировало.
Иными словами, если в исходном субстрате левосторонних аминокислот будет чуть больше, то высокая скорость реакции соединения левосторонних аминокислот с правосторонними быстро истощит правосторонние. Вследствие этого растет концентрация левосторонних молекул.
Вдобавок гетерохиральные пептиды слипались и выпадали в осадок, оставляя в смеси только гомохиральные L-аминокислоты. Самое удивительное, по словам авторов, что добавление ахирального катализатора (то есть молекул тиола, которые могут совмещаться) вызвала ту же селективность пептидов в реакции, что и левосторонний катализатор. Как отмечают исследователи, этот факт делает такую систему возникновения гомохиральности в пребиотических условиях более вероятной.
Популярные категории
Популярные статьи

Космонавтика
Японский лунный аппарат SLIM неожиданно вышел на связь из перевернутого положения 29.01.2024


Медицина
Алкоголь на ночь изменил структуру сна 29.01.2024
Биология
Ученые впервые увидели попытку шмелей вылечить свои раны 29.01.2024